【骨折處理】港大醫學院研究:鎂離子免疫調控機制有效促進骨骼癒合 助研發治療骨折精準療程
鎂離子具細胞新陳代謝、促進成骨作用
在骨骼組織中,鎂離子作為一種重要的微量礦物質元素,因此醫學研究就鎂離子在細胞新陳代謝、促進成骨的作用已有廣泛報導,但在複雜的骨折癒合過程中(包括骨骼組織炎症反應、骨骼重建及重塑等階段),鎂離子的角色尚未得到有系統的剖析。
另外,生物學研究發現單核巨噬細胞體系在外界刺激下,可通過調控體內微環境,影響骨骼的代謝平衡。
有見及此,研究團隊模擬了由單核巨噬細胞在骨折修復中所引發的多種免疫反應場景,在不同階段導入了鎂離子作為治療。研究發現,在骨骼癒合的不同階段,可透過適度調整鎂離子的濃度,來控制骨骼再生的速度和質素。
研究團隊選用大鼠股骨缺損模型開展研究。在不同的骨骼修復階段中,研究人員把可釋放鎂離子的海藻酸鹽水凝膠注射到大鼠體內。結果顯示,鎂離子僅在骨骼修復初期(手術後1至7天)表現出顯著促成新骨生長的作用,但延遲或持續提高鎂離子濃度,卻會大幅減弱新骨生長的速度和質素,相差可超過2.5倍。
在另一項實驗中,團隊透過在大鼠腹腔注射氯膦酸二鈉脂質體,敲除了大鼠模型中的巨噬細胞所引起的免疫反應後,鎂離子的成骨作用亦不復存在。因此,研究團隊認為鎂離子的成骨作用,是經由巨噬細胞調控和引導的。
體外實驗進一步證明鎂離子濃度上升,可顯著提高巨噬細胞內的鎂離子濃度,並增加與鎂離子相關的TRPM7的表達。然而在後期骨骼重建階段,持續釋放過量鎂離子,將導致NF-κB信號通路過度活躍,增加了破骨細胞數量,同時抑制羥基磷灰石(骨組織中的重要成分)的沉積,反而降低了骨組織的癒合速度及能力。這些不良作用,甚至抵銷了鎂離子在早期促進骨骼生長的功效。
領導是次研究的港大醫學院矯形及創傷外科學系楊偉國教授表示:「是次研究結果帶出了一項非常重要的訊息,就是如要骨骼癒合理想,在使用如鎂等有助骨質生長的礦物質時,也要講究時機和劑量準確,否則只會適得其反。我們會繼續研究不同礦物質在骨骼癒合中的作用、使用時機和劑量等,以便研發更有效、更精準治療骨折的方法,將來或可用於處理骨質疏鬆等其他骨骼問題。」
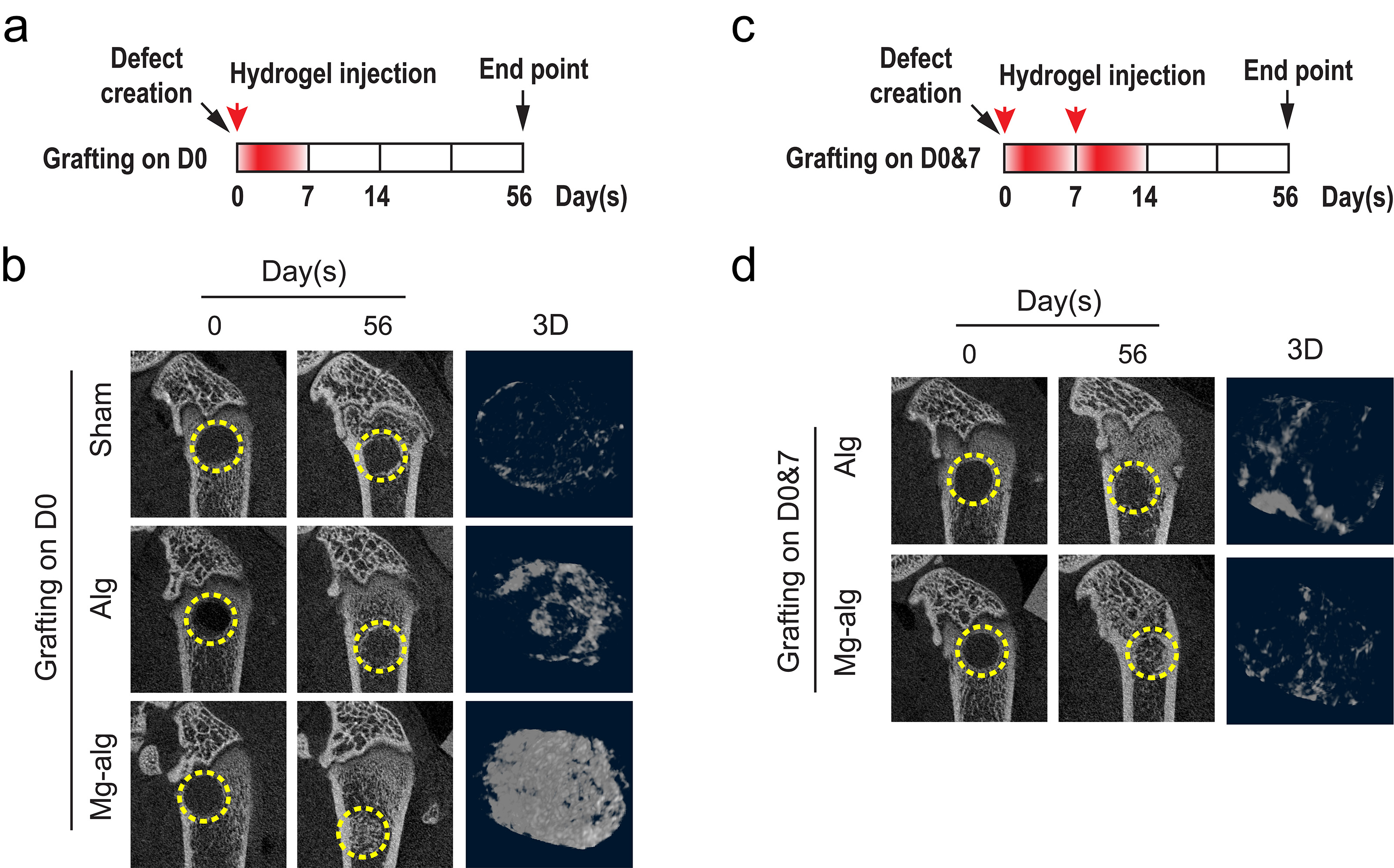 Photo from 港大醫學院
Photo from 港大醫學院
Text : UrbanLife Health Editorial
Photos : UrbanLife Health Editorial